两项突破性研究:切断胰腺癌细胞的复制增殖之路
胰腺癌是一种非常难以治疗的恶性肿瘤,其早期诊断困难且预后效果差,发病率和死亡率高居全球和中国恶性肿瘤的前十位。
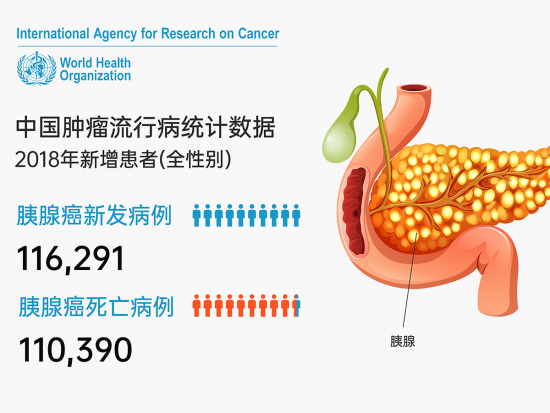
为了攻克胰腺癌,来自希望之城的 Mustafa Raoof 博士正在从根本上寻找一些突破方式来切断癌细胞的复制过程:利用癌细胞 DNA 复制与转录过程中的“碰撞”来抑制癌细胞的复制;利用前沿药物靶向增殖细胞核抗原(PCNA)杀灭胰腺癌细胞。
由于胰腺癌细胞可以不断的复制和增殖,因此科学家们需要破解的寻找一种方法,去破坏其复制过程,这也是 Raoof 博士正在研究的重点,他也因此一举获得了两项大奖:胰腺癌行动网(PanCAN)职业发展奖和来自美国国家综合癌症网 (NCCN)的青年研究者奖。
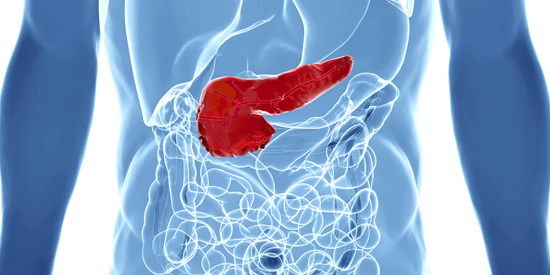
“这是世界上最难治疗的癌症之一,因为大多数患者的生存期非常有限,我们必须开发新的疗法。”他告诉我们:“我很荣幸他们在我们的研究中看到了一些希望,而且我们的研究重点非常让人感兴趣。”这些奖助将支持 Raoof 博士研究治疗这种疾病的两种新方法,我们就他工作背后的创新科学与他进行了交谈。
利用癌细胞复制过程中的DNA损伤来抑制癌细胞复制
胰腺癌细胞是名副其实的“生存大师”,即使在治疗后受到严重损害的它们仍能自我复制和增殖。事实上,它们往往会因此而变得更加强大。但在这一过程中也埋藏着它们自身毁灭的种子——这就是 PanCAN 研究将要探索的地方。
为了让细胞复制,它们必须首先复制自己的 DNA。这需要一套由数十种蛋白质组成的特殊分子机器。这些蛋白质像拉链一样附着在 DNA 模板上并沿着模板运行,从而读取遗传密码,并高精度地进行复制。
在它们沿着 DNA 运行的过程中,复制机器遇到了一组不同的分子机器。这些分子机器参与了一个同样重要但独立的、被称作“转录”的过程。转录机器将储存在 DNA 中的信息复制成信使 RNA,后者最终被用来生成细胞中各种功能所需的蛋白质。
但这里有一个漏洞,那就是这两台机器可能会碰撞到彼此。“转录机比复制机慢 100 倍。”Raoof 博士解释道,“当它们相撞时,就像超速行驶的汽车撞向行人,从而造成严重的损害。” 增加这种损害可能是治疗癌症的一种方法,但这只是故事的一半。
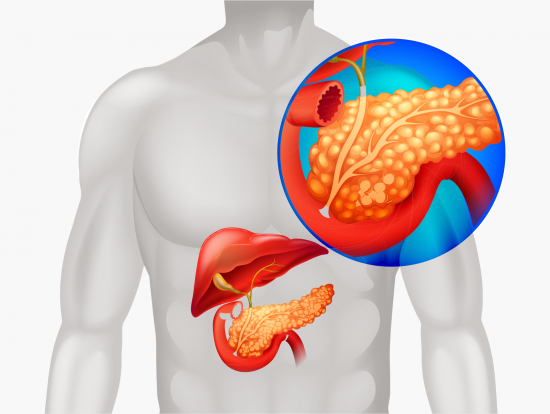
“长期以来,我们一直采用化学疗法来抑制癌细胞发生复制,结果癌症还是会复发。所以仅仅针对复制过程是不够的。由于我们对于细胞是如何解决这些碰撞知之甚少,因此这是一个令人兴奋的问题。”
由于癌症不断复制,两种分子机器碰撞就会变得非常频繁,这对细胞来说具有杀伤力——但它们也有办法避免这样的碰撞。正常细胞也会这样做,但不经常使用它们,所以针对碰撞避免机制可能对癌细胞是致命的,而不会伤害健康细胞。
Raoof 博士的研究将探索胰腺癌用来解决碰撞的机制,以学习如何阻止癌细胞的复制过程——换句话说,就是关闭红绿灯。如果他能做到这一点,碰撞就会升级,DNA 损伤不仅可以杀死恶性细胞,而且还会阻止它们发生复制。他的具体目标是发现哪种类型的癌细胞最依赖于避碰机制,以及这些机制中哪些蛋白质会对药物产生反应。

利用前沿药物靶向增殖细胞核抗原(PCNA)杀灭胰腺癌细胞
NCCN 的这份研究报告是在 Raoof 博士最近与希望之城转化科学系主任Linda Malkas博士完成的概念验证研究基础上进行的。这项发表在《分子治疗溶瘤学》上的研究结果表明,在实验室模型中,靶向一种名为增殖细胞核抗原(PCNA)的复制和修复蛋白,可以杀死胰腺癌细胞。
他们的研究证明,实验室制造的一种名为 R9-caPeptide 的物质可以破坏 PCNA 与其结合物之间的相互作用。这种破坏在癌细胞中是有毒的,但在正常细胞中则没有。然而,R9-caPeptide 不能轻易转化为药物。在一项对比研究中,Raoof 博士采用了由 Malkus 博士开发的新药 AOH1996 进行替代。这种新药是一种能结合 PCNA 的小分子抑制剂,在治疗乳腺癌等其他类型的癌症上已经取得了令人满意的效果。这项研究表明,它对胰腺癌同样有效,研究结果将出现在一篇即将出版的论文中。

但相关实验仍需进一步研究,而这正是 NCCN 奖项将要涵盖的内容。“在癌症中,没有什么是 100% 可以确定的,所以 AOH1996 在一些细胞系和模型中起作用,但在其他的细胞系和模型中却不起作用,因此,这项研究将探索它究竟是如何以及为什么起作用或不起作用的。
相关阅读

最新文章
随机推荐
- 瘦身专访“菩提子瘦身茶”瘦身的同时还要赚分红
- 全棉空间倡导自然健康生活方式
- 蜜蜂电台:关于儿童口才表达这些常识父母要知晓
- 喜迎开业!医庄吾知爱产康中心盛大开业!
- 御宝臻启新鲜好羊奶 孩子成长发育好帮手
- 波后轻悦纤体塑形计划,女性不容错过的好项目!
- 夏季失眠焦虑情况增多 夜然舒植物调理更安全
- 日本一众明星夫妇推荐的花取HEEKOI屁屁霜什么来头?
- 眼鼻培训基地成立 天津伊美尔树立隆鼻安全新标准
- 水之典果蔬净,放心吃瓜 放心吃菜
- 荣和唯真氨基酸维生素功能饮品正式上线苏宁众筹平台,上线时间30天
- COVID-19 疫情期间,肺癌患者的健康管理
- 2017,众乡园——奉节脐橙为您守护健康
- Hitacea(医图亚)让大健康产业在联邦学习下有所惠民,让你的健康一步到位
- 肾不好,早知道,康云教你看你指标
- 点滴呵护 美到脱俗 植佩兰值得你的信赖
- 靓齿蜜码推动国家健康产业发展,助力全民口腔健康生活!
- 在家办公如何合理用眼?
- 石汉平教授与丽丽卡女士共同探讨肿瘤患者营养问题
- 科技创新是第一驱动力,爱啦无忧引领大健康产业的技术创新




最新评论
更多评论